UEL 2011 Química - Questões
Abrir Opções Avançadas
Se, no decorrer de uma atividade esportiva, um atleta necessitar de mais oxigênio, poderá utilizar uma máscara contendo superóxido de potássio, que reage com o gás carbônico e com a água exalados por ele para formar o gás oxigênio. A equação química do processo é mostrada a seguir.
$$4KO_{2\ (s)} + 2H_2O_{(g)} + 4CO_{2\ (g)} \to 4KHCO_{3\ (s)} + 3O_{2\ (g)}$$
Dados:
Massas molares ($\text{g/mol}$): $H = 1, 00$; $C = 12, 0$; $O = 16, 0$; $K = 39, 0$
Se esse atleta exalar $0,62\ \text{g}$ de gás carbônico por minuto, a massa, em gramas, de superóxido de potássio consumida em $10,0\ \text{minutos}$ será:
Durante atividades físicas, o aumento da temperatura do corpo e a consequente transpiração promovem a oxidação de gorduras acumuladas sobre a pele. As equações químicas de oxidação do ácido oleico, gordura presente na pele, são mostradas a seguir.

Dado: Temperatura de fusão do ácido oleico = $14\ ^\circ \text{C}$ Com base no enunciado e nas equações químicas, assinale a alternativa correta.
As bebidas isotônicas, muito utilizadas por atletas, foram desenvolvidas para repor líquidos e sais minerais perdidos pelo suor durante a transpiração. Um determinado frasco de $500\ \text{mL}$ desta bebida contém $225\ \text{mg}$ de íons sódio, $60,0\ \text{mg}$ de íons potássio, $210\ \text{mg}$ de íons cloreto e $30,0\ \text{g}$ de carboidrato.
Com relação aos íons presentes nesse frasco, é correto afirmar:
Dados: Número de Avogrado = $6,0 \times 10^{23}$ Número atômico $Na = 11$; $C\ell = 17$; $K = 19$ Massas molares ($\text{g/mol}$) $Na = 23,0$; $C\ell = 35,5$; $K = 39,0$
Considere a equação química a seguir e assinale a alternativa que completa corretamente o texto.
$$CO_{2\ (g)} + H_2O_{(l)} \rightleftarrows H_2CO_{3\ (aq)} \rightleftarrows H^+_{(aq)} + HCO^-_{3\ (aq)}$$
Durante um exercício físico prolongado, quando a respiração aumenta, a concentração de dióxido de carbono diminui e o sangue torna-se mais __________. Por outro lado, numa situação de repouso, a respiração diminui, a concentração de dióxido de carbono aumenta e o sangue torna-se mais __________. O pH sanguíneo é regulado constantemente e seu valor normal está situado entre 7,35 a 7,45, sendo ligeiramente __________. Uma alteração no controle do pH pode alterar o equilíbrio ácido-base produzindo a acidose ou a alcalose. A acidose é quando o sangue apresenta um excesso de ácido, acarretando uma __________ do pH sanguíneo e a alcalose é quando o sangue apresenta um excesso de base, acarretando uma __________ do pH sanguíneo.
As bolsas instantâneas, frias ou quentes, usadas nos atletas que sofrem distensões musculares, dividem-se em dois compartimentos: um contendo água líquida e outro contendo um sal, que absorve ou libera calor quando em contato com a água.
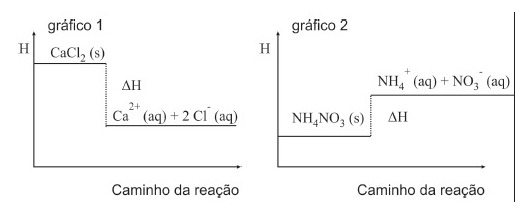
As reações químicas que ocorrem nas bolsas instantâneas são representadas nos gráficos a seguir. Com base no enunciado e nos conhecimentos sobre calor de reação, é correto afirmar:
Carregando...