São fornecidas as seguintes informações a respeito de titulação ácido-base:
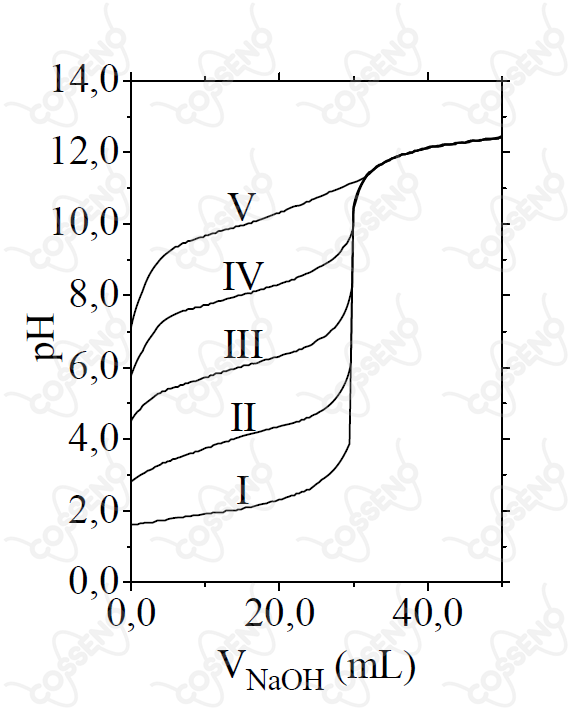
a) A figura mostra as curvas de titulação de de diferentes ácidos (I, II, III, IV e V), todos a , com uma solução aquosa em .
b) O indicador fenolftaleína apresenta o intervalo de mudança de cor entre pH a , e o indicador vermelho de metila, entre pH a . Considerando estas informações, é CORRETO afirmar que
CossenoGPT
Teste
gratuitamente agora
mesmo! 

$• \ \text{Alternativa (A):}$ $\color{orangered}{\text{Incorreta}}$
O ácido $\text{IV}$ é claramente um ácido fraco, devido seu alto $\ce{pH}$ na ausência de base. Nesse sentido, devemos olhar para seu ponto de equivalência, a variação deste é sutil devido a fragilidade do ácido, estando entre $9,0-11,0$. Dessa forma, torna-se inviável o uso do vermelho de metila, pois ele seria incapaz de indicar o ponto de equivalência, já que sua mudança de cor está entre $4,0-6,0$.
$• \ \text{Alternativa (B):}$ $\color{orangered}{\text{Incorreta}}$
Raciocínio análogo ao anterior.
$• \ \text{Alternativa (C):}$ $\color{orangered}{\text{Incorreta}}$
Observe o ponto em que há ausência de base, o $\ce{pH}$ do ácido $\text{III}$ é maior que o de $\text{II}$. Portanto, o ácido $\text{III}$ é mais fraco que o de $\text{II}$.
$• \ \text{Alternativa (D):}$ $\color{#3368b8}{\text{Correta}}$
Analisando a variação do ponto de equivalência (ou o $\text{pH}$), podemos inferir que estamos tratando de um ácido forte. Com isso, repare quão abrupta é a variação, isto mostra que diversos indicadores poderiam ser utilizados, assim como os dois listados, visto que estão presentes no intervalo em questão.
$• \ \text{Alternativa (E):}$ $\color{orangered}{\text{Incorreta}}$
O raciocínio é análogo ao que foi dito anteriormente, no caso, o vermelho de metila seria inviável.\begin{matrix}Letra \ (D)
\end{matrix}

