Uma porção de certo líquido, contido numa garrafa térmica sem tampa, é aquecido por uma resistência elétrica submersa no líquido e ligado a uma fonte de potência constante. O que se nota é mostrado no gráfico a seguir. 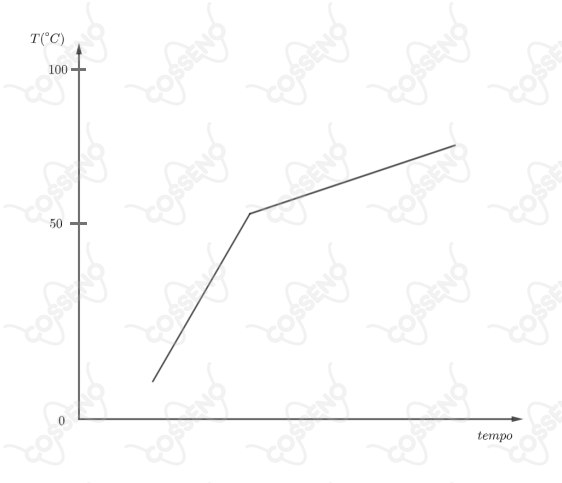
Considerando o local onde a experiência é realizada, este líquido poderia ser:
CossenoGPT
Teste
gratuitamente agora
mesmo! 

$• \ \text{Afirmativa (A):}$ $\color{orangered}{\text{Incorreta}}$
Uma substância pura não apresentaria uma inflexão como há no gráfico.
$• \ \text{Afirmativa (B):}$ $\color{orangered}{\text{Incorreta}}$
A presença de soluto aumenta o ponto de ebulição, pois dificulta a tendência ao escape da solução, isto é, a água deveria ebulir a mais de $100^{\circ}C$.
$• \ \text{Afirmativa (C):}$ $\color{royalblue}{\text{Correta}}$
A repentina inflexão no gráfico provavelmente se refere a uma mistura, poderíamos dizer que a acetona começa a ebulir próximo dos $56^{\circ}C$. Além disso, água e acetona são miscíveis, a mistura de água com um soluto mais volátil que ela é suficiente para que a solução apresente uma menor temperatura de ebulição que a água pura. Atente que, normalmente, numa mistura miscível, o ponto de ebulição fica entre os dos dois componentes.
$\color{orangered}{Obs:}$ A mistura de água e acetona não é capaz de produzir um azeótropo normalmente (apenas em certa tempertura e pressão), então realmente teríamos a descontinuidade.
$• \ \text{Afirmativa (D):}$ $\color{orangered}{\text{Incorreta}}$
Uma substância pura não apresentaria uma inflexão como há no gráfico, além de que, a acetona pura iria entrar em ebulição próximo de $56^{\circ}C$.
$• \ \text{Afirmativa (E):}$ $\color{orangered}{\text{Incorreta}}$
Vide explicações anteriores, ainda poderíamos acrescentar o fato que, ao ir abaixo do nível do mar, faríamos o ponto de ebulição da água aumentar. \begin{matrix} Letra \ (C)
\end{matrix}

