Um copo contém, inicialmente, de uma solução aquosa molar de uma substância desconhecida. De uma bureta se deixa cair, gota a gota, uma solução aquosa molar de outra substância, também desconhecida. Sabe-se que uma das substâncias em questão é um ácido e a outra uma base. Após a adição de cada gota da bureta, o pH do conteúdo do copo é monitorado e o resultado desta monitoração do pH é mostrado no gráfico a seguir. 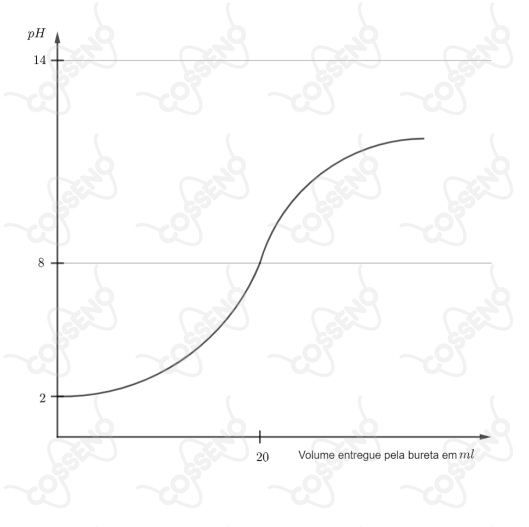
Da observação do gráfico acima, qual era a natureza das soluções iniciais no copo e na bureta, respectivamente?
CossenoGPT
Teste
gratuitamente agora
mesmo! 

A priori, quando há apenas a substância do copo, nota-se o $\ce{pH = 2}$, o que indica a maior concentração de hídrons, consequentemente, uma solução ácida. Nesse escopo, estamos falando de titulações, em que é importante verificar o ponto de equivalência, pois, se estivéssemos falando de ácidos e bases fortes, o $\ce{pH}$ deveria ser $7$ neste ponto, mas não é, ele é $8$, o que diz haver uma base mais forte que o ácido, visto que na equivalência a base prevalece. Portanto, constatamos que há um ácido fraco no copo, enquanto existe uma base forte na bureta.\begin{matrix}Letra \ (C)
\end{matrix}$\text{Comentário:}$ É importante ter conhecimento dos gráficos em processos de titulação, visto que as curvas em questão são bem características. Por exemplo, com ácidos e bases fortes, o ponto de equivalência apresenta uma variação extremamente brusca. Por outro lado, processos com ácidos fortes junto de bases fracas e vice-versa, apresentam, normalmente, variações muito mais "suaves" como a do gráfico.

17:29 30/01/2023
Boa tarde, Anderson! A resolução está certa, a questão estava com gabarito errado. Já corrigimos, agora consta letra (C). Obrigado e bons estudos! 🚀


