UNESP 2018 Química - Questões
Abrir Opções Avançadas
A pilha $Ag-Zn$ é bastante empregada na área militar (submarinos, torpedos, mísseis), sendo adequada também para sistemas compactos. A diferença de potencial desta pilha é de cerca de 1,6 V à temperatura ambiente. As reações que ocorrem nesse sistema são:
$$\begin{array}{ll} \text{No cátodo:} & Ag_2O+H_2O+2e^-\ \to\ 2Ag+2OH^- \\ \text{No ânodo:} & Zn\ \to\ Zn^{2+}+2e^- \\ & Zn^{2+}+2OH^-\ \to\ Zn(OH)_2 \\ \text{Reação global:} & Zn+Ag_2O+H_2O\ \to\ 2Ag+Zn(OH)_2 \end{array}$$
(Cristiano N. da Silva e Julio C. Afonso. “Processamento de pilhas do tipo botão”. Quím. Nova, vol. 31, 2008. Adaptado.)
a) Identifique o eletrodo em que ocorre a semirreação de redução. Esse eletrodo é o polo positivo ou o negativo da pilha?
b) Considerando a reação global, calcule a razão entre as massas de zinco e de óxido de prata que reagem. Determine a massa de prata metálica formada pela reação completa de 2,32 g de óxido de prata.
No interior de uma célula mantida a $40^\circ\text{C}$ ocorreu uma reação bioquímica enzimática exotérmica. O gráfico $1$ mostra a energia de ativação ($E_a$) envolvida no processo e o gráfico $2$ mostra a atividade da enzima que participa dessa reação, em relação à variação da temperatura.
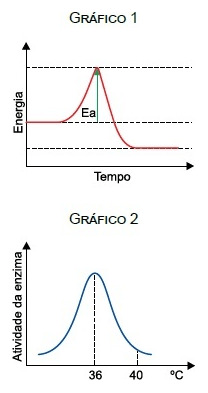
Se essa reação bioquímica ocorrer com a célula mantida a $36^\circ\text{C}$, a energia de ativação ($E_a$) indicada no gráfico $1$ e a velocidade da reação serão, respectivamente,
O quadro fornece indicações sobre a solubilidade de alguns compostos iônicos inorgânicos em água a $20^\circ\text{C}$.
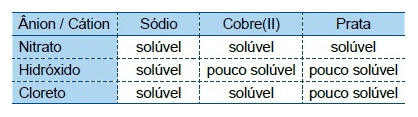
Em um laboratório, uma solução aquosa obtida a partir da reação de uma liga metálica com ácido nítrico contém nitrato de cobre (II) e nitrato de prata. Dessa solução, pretende-se remover, por precipitação, íons de prata e íons de cobre (II), separadamente. Para tanto, pode-se adicionar à mistura uma solução aquosa de
Considere os elementos $K$, $Co$, $As$ e $Br$, todos localizados no quarto período da Classificação Periódica. O elemento de maior densidade e o elemento mais eletronegativo são, respectivamente,
Bicarbonato de sódio sólido aquecido se decompõe, produzindo carbonato de sódio sólido, além de água e dióxido de carbono gasosos. O gráfico mostra os resultados de um experimento em que foram determinadas as massas de carbonato de sódio obtidas pela decomposição de diferentes massas de bicarbonato de sódio.
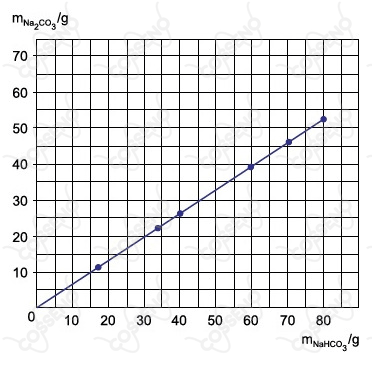
Os dados do gráfico permitem concluir que as massas de carbonato de sódio e bicarbonato de sódio nessa reação estão relacionadas pela equação $m_{Na_2CO_3} = k\cdot m_{NaHCO_3}$ e que o valor aproximado de $k$ é
Carregando...