Considere de uma solução tampão aquosa () que contém de ácido benzóico (). A fim de extrair o ácido dessa solução, utiliza-se o mesmo volume de um solvente orgânico imiscível em água. A mistura é agitada, deixada em repouso e, após a separação de fases, atinge o equilíbrio ():
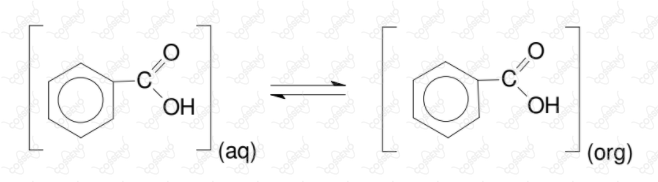
Na fase orgânica, o ácido benzóico não se dissocia, mas sofre o seguinte processo de dimerização parcial ():
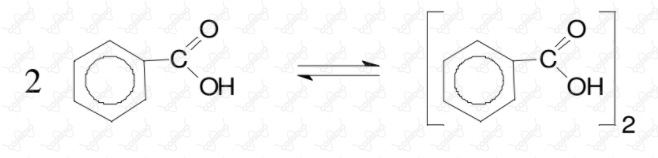
Calcule a concentração final do ácido benzóico na fase aquosa após a extração descrita acima.
$\Delta H_{f}^{\circ}\;(Fe(s)):\;0\;kJ.mol^{-1}$
$\Delta H_{f}^{\circ}\;(Fe_3C(s)):\;25,10\;kJ.mol^{-1}$
$\Delta H_{f}^{\circ}\;(CH_4(g)):\;-74,80\;kJ.mol^{-1}$
$\Delta H_{f}^{\circ}\;(H_2(g)):\;0\;kJ.mol^{-1}$
$\Delta S_{f}^{\circ}\;(Fe(s)):\;27,30\;J.mol^{-1}$
$\Delta S_{f}^{\circ}\;(Fe(s)):\;104,6\;J.mol^{-1}$
$\Delta S_{f}^{\circ}\;(Fe(s)):\;186,2\;J.mol^{-1}$
$\Delta S_{f}^{\circ}\;(Fe(s)):\;130,6\;J.mol^{-1}$