USP 2010 Química - Questões
Abrir Opções Avançadas
Cloreto de nitrosila puro $(NOC\ell )$ foi aquecido a $240\ ^\circ C$ em um recipiente fechado. No equilíbrio, a pressão total foi de 1,000 atm e a pressão parcial do $NOC\ell$ foi de $0,640\ atm$.
A equação abaixo representa o equilíbrio do sistema:
$$2\ NOC{\ell }_{(g)}\ \ \rightleftarrows \ \ 2\ NO_{(g)}\ +\ C{\ell }_{2(g)}$$
a) Calcule as pressões parciais do $NO$ e do $C{\ell }_2$ no equilíbrio.
b) Calcule a constante do equilíbrio.
Determinou-se o número de moléculas de água de hidratação $(x)$ por molécula de ácido oxálico hidratado $(H_2C_2O_4\cdot xH_2O)$, que é um ácido dicarboxílico. Para isso, foram preparados $250\ mL$ de uma solução aquosa, contendo $5,04\ g$ de ácido oxálico hidratado. Em seguida, $25,0\ mL$ dessa solução foram neutralizados com $16,0\ mL$ de uma solução de hidróxido de sódio, de concentração $0,500\ mol/L$.
Dados:
Massas molares ($g/mol)$: $H=1$; $C=12$; $O=16$
a) Calcule a concentração, em mol/L, da solução aquosa de ácido oxálico.
b) Calcule o valor de $x$.
A proporção do isótopo radioativo do carbono $(^{14}C)$, com meia-vida de, aproximadamente, 5.700 anos, é constante na atmosfera. Todos os organismos vivos absorvem tal isótopo por meio de fotossíntese e alimentação. Após a morte desses organismos, a quantidade incorporada do $\ ^{14}C$ começa a diminuir exponencialmente, por não haver mais absorção.
a) Balanceie a equação química da fotossíntese, reproduzida abaixo, e destaque nela o composto em que o $\ ^{14}C$ foi incorporado ao organismo. $$\_\_\_\_CO_2+\_\_\_\_H_2O\ \ {{\stackrel{luz\ solar}{\longrightarrow}}}\_\_\_\_C_6H_{12}O_6+\_\_\_\_H_2O+\_\_\_\_O_2$$
b) Por que um pedaço de carvão que contenha 25% da quantidade original de $\ ^{14}C$ não pode ser proveniente de uma árvore do início da era cristã?
c) Por que não é possível fazer a datação de objetos de bronze a partir da avaliação da quantidade de $\ ^{14}C$?
Na produção de combustível nuclear, o trióxido de urânio é transformado no hexafluoreto de urânio, como representado pelas equações químicas:
I. $UO_{3\ (s)}+H_{2\ (g)}\ \longrightarrow\ UO_{2\ (s)}+H_2O_{(g)}$
II. $UO_{2\ (s)}+4HF_{(g)}\ \longrightarrow\ UF_{4\ (s)}+2H_2O_{(g)}$
III. $UF_{4\ (s)}+F_{2\ (g)}\ \longrightarrow\ UF_{6\ (g)}$
Sobre tais transformações, pode-se afirmar, corretamente, que ocorre oxirredução apenas em
Um estudante desejava estudar, experimentalmente, o efeito da temperatura sobre a velocidade de uma transformação química. Essa transformação pode ser representada por:
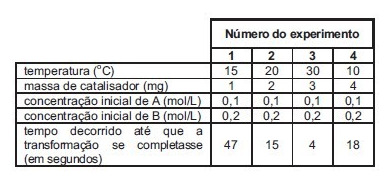
Após uma série de quatro experimentos, o estudante representou os dados obtidos em uma tabela:

Que modificação deveria ser feita no procedimento para obter resultados experimentais mais adequados ao objetivo proposto?
Carregando...