UNIFESP 2006 Química - Questões
Abrir Opções Avançadas
Existem diferentes formas pelas quais a água pode fazer parte da composição dos sólidos, resultando numa grande variedade de substâncias encontradas na natureza que contêm água ou elementos que a formam. A água de estrutura é denominada de água de hidratação, que difere muito da água de absorção ou adsorção. A água de constituição é uma forma de água em sólidos, que é formada quando estes se decompõem pela ação de calor.
a) O $NaHCO_3$ e $Ca(OH)_2$ são sólidos que apresentam água de constituição. Escreva as equações, devidamente balanceadas, que evidenciam essa afirmação, sabendo-se que na decomposição do bicarbonato de sódio é produzido um óxido de caráter ácido.
b) No tratamento pós-operatório, um medicamento usado para estimular a cicatrização é o sulfato de zinco hidratado, $ZnSO_4\cdot xH_2O$. A análise desse sólido indicou 43,9% em massa de água. Determine neste composto o número de moléculas de água por fórmula unitária.
Dadas massas molares ($\text{g/mol}$): $ZnSO_4 = 161,5$ e $H_2O = 18,0$.
60 anos após as explosões das bombas atômicas em Hiroshima e Nagasaki, oito nações, pelo menos, possuem armas nucleares. Esse fato, associado a ações terroristas, representa uma ameaça ao mundo. Na cidade de Hiroshima foi lançada uma bomba de urânio-235 e em Nagasaki uma de plutônio-239, resultando em mais de cem mil mortes imediatas e outras milhares como consequência da radioatividade. As possíveis reações nucleares que ocorreram nas explosões de cada bomba são representadas nas equações: $$\ ^{235}_{92}U+^1_0n\to ^{142}_zX+^{91}_{36}{Kr}+3^1_0n$$ Nas equações, $Z$, $X$, $A$ e o tipo de reação nuclear são, respectivamente,
A bateria primária de lítio-iodo surgiu em 1967, nos Estados Unidos, revolucionando a história do marca-passo cardíaco. Ela pesa menos que$\ 20\ g$ e apresenta longa duração, cerca de cinco a oito anos, evitando que o paciente tenha que se submeter a frequentes cirurgias para trocar o marca-passo. O esquema dessa bateria é representado na figura ao lado.
Para esta pilha, são dadas as semirreações de redução:
$$Li^++e^-\to Li\qquad E^0=-3,05\ \text{V}$$ $$I_2+2e^-\to 2I^-\qquad E^0=+0,54\ \text{V}$$
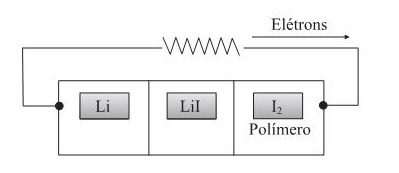
São feitas as seguintes afirmações sobre esta pilha:
I) No ânodo ocorre a redução do íon $Li^+$.
II) A ddp da pilha é $+ 2,51\ \text{V}$.
III) O cátodo é o polímero/iodo.
IV) O agente oxidante é o $I_2$.
São corretas as afirmações contidas apenas em
Medicamentos obtidos da natureza são utilizados pelo homem há muito tempo. Produtos naturais e seus derivados são muito empregados na fabricação de medicamentos pelas indústrias farmacêuticas modernas. A maio- ria das pessoas, em algum momento, já fez uso de alguns desses compostos. O ácido acetilsalicílico, estrutura representada na figura, que compõe o conhecido medicamento de nome comercial aspirina, é obtido a partir do ácido salicílico que ocorre na casca da árvore do salgueiro branco, Salix alba.
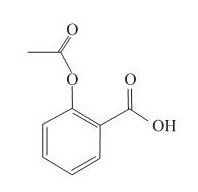
Na hidrólise da aspirina é formada uma substância que está presente no vinagre e também o ácido salicílico, que tem fórmula molecular
Em intervenções cirúrgicas, é comum aplicar uma tintura de iodo na região do corpo onde será feita a incisão. A utilização desse produto deve-se à sua ação antisséptica e bactericida. Para 5 litros de etanol, densidade 0,8 g/mL a massa de iodo sólido, em gramas, que deverá ser utilizada para obter uma solução que contém $0,50\ \text{mol}$ de $I_2$ para cada quilograma de álcool, será de
Carregando...