UNESP 2020 Química - Questões
Abrir Opções Avançadas
O Brasil já é o segundo país que mais realiza a cirurgia bariátrica, que reduz o tamanho do estômago.
O paciente consegue emagrecer porque perde a fome radicalmente - a quantidade de comida consumida cai a um quarto, em média, por falta de espaço. Apesar dos avanços técnicos e das facilidades, a cirurgia está longe de ser uma intervenção simples.
(Natalia Cuminale. "Emagrecer na faca". Veja, 13.03.2019. Adaptado.)
Além de aumentar a sensação de saciedade, mesmo com pequena ingestão de alimentos, a redução do estômago também reduz a quantidade de suco gástrico secretado pela parede estomacal, comprometendo a digestão do alimento nessa porção do aparelho digestório.
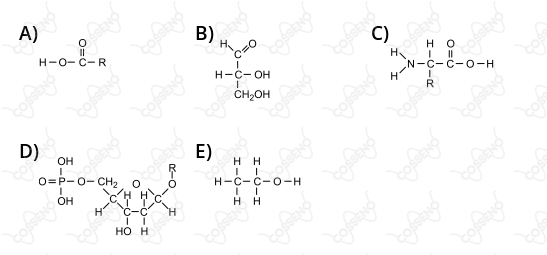
A principal enzima digestória do suco gástrico e a estrutura química dos monômeros das moléculas sobre as quais atua são
Um estudante coletou informações sobre a concentração total de sais dissolvidos, expressa em diferentes unidades de medida, de quatro amostras de águas naturais de diferentes regiões. Com os dados obtidos, preparou a seguinte tabela:
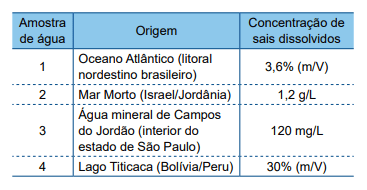
Ao rever essa tabela, o estudante notou que dois dos valores de concentração foram digitados em linhas trocadas. Esses valores são os correspondentes às amostras
Parque Eólico de Osório, RS

(https://1.bp.blogspot.com/-w-CnSCkfy7U/XdBjYXoVF-/AAAAAAACYtE/NWQNHC8RcKwlfRWHn7-pXt9ZSV4VQ-ryQCLcBGAsYHQ/s1600/unesmp2020-q70.jpg)
O Parque Eólico de Osório é o maior da América Latina e o segundo maior do mundo em operação. Com capacidade produtiva total de $150 \ \text{MW}$, tem potência suficiente para abastecer anualmente o consumo residencial de energia elétrica de cerca de $650\text{ mil pessoas}$.
(www.osorio.rs.gov.br. Adaptado.)
Considere agora a combustão completa do metano, principal componente do gás natural, cuja entalpia de combustão completa é cerca de $-9 \times 10^2\ \text{kJ/mol}$, e que as transformações de energia nessa combustão tenham eficiência ideal, de $100\%$.
Para fornecer a mesma quantidade de energia obtida pelo Parque Eólico de Osório quando opera por $1$ hora com sua capacidade máxima, uma usina termoelétrica a gás necessitaria da combustão completa de uma massa mínima de metano da ordem de
As antocianinas existem em plantas superiores e são responsáveis pelas tonalidades vermelhas e azuis das flores e frutos. Esses corantes naturais apresentam estruturas diferentes conforme o $pH$ do meio, o que resulta em cores diferentes.
O cátion flavílio, por exemplo, é uma antocianina que apresenta cor vermelha e é estável em $pH \approx 1$. Se juntarmos uma solução dessa antocianina a uma base, de modo a ter pH por volta de 5, veremos, durante a mistura, uma bonita cor azul, que não é estável e logo desaparece.
Verificou-se que a adição de base a uma solução do cátion flavílio com $pH \approx 1$ dá origem a uma cinética com 3 etapas de tempos muito diferentes. A primeira etapa consiste na observação da cor azul, que ocorre durante o tempo de mistura da base. A seguir, na escala de minutos, ocorre outra reação, correspondendo ao desaparecimento da cor azul e, finalmente, uma terceira que, em horas, dá origem a pequenas variações no espectro de absorção, principalmente na zona do ultravioleta.
(Paulo J. F. Cameira dos Santos et al. “Sobre a cor dos vinhos: o estudo das antocianinas e compostos análogos não parou nos anos 80 do século passado”. www.iniav.pt, 2018. Adaptado.)
A variação de $pH$ de $\approx 1$ para $\approx 5$ significa que a concentração de íons $H^+(aq)$ na solução ____, aproximadamente, ____ vezes. Entre as etapas cinéticas citadas no texto, a que deve ter maior energia de ativação e, portanto, ser a etapa determinante da rapidez do processo como um todo é a ____.
As lacunas do texto são preenchidas, respectivamente, por:
Considere um cubo de aço inoxidável cujas arestas medem 1 cm.
Deseja-se recobrir as faces desse cubo com uma camada uniforme de cobre de $1 \cdot 10^{–2}\ \text{cm}$ de espessura. Para isso, o cubo pode ser utilizado como cátodo de uma cuba eletrolítica contendo íons $Cu^{2+} (aq)$. Admita que a eletrólise se realize sob corrente elétrica de $200\ \text{mA}$, que a constante de Faraday seja igual a $1 \cdot 10^5\ \text{C/mol}$ e que a densidade do cobre seja $9\ \text{g/cm}^3$. Assim, estima-se que o tempo de eletrólise necessário para que se deposite no cubo a camada de cobre deseja- da será próximo de
Carregando...