Filtro de Questões
Abrir Opções Avançadas
Com base nos elementos da tabela periódica e seus compostos, considere as seguintes afirmativas:
1. Elementos que apresentam baixos valores da primeira energia de ionização, mas altos valores de afinidade eletrônica são considerados bastante eletronegativos.
2. Os compostos gerados por elementos de baixa eletronegatividade possuem caráter metálico.
3. Os compostos gerados por elementos de alta eletronegatividade possuem caráter covalente.
4. Os elementos representativos que possuem valores mais altos da primeira energia de ionização são os mais eletronegativos.
Assinale a alternativa correta.
As plantas sintetizam a estrutura de poliisopreno das borrachas naturais usando o pirofosfato de 3-metilbut-3-enila. Muitos outros produtos naturais são derivados desse composto, incluindo os terpenos. O sesquiterpeno farnesol é uma das substâncias mais comuns do reino vegetal e é um precursor biossintético da estrutura de esteroides.
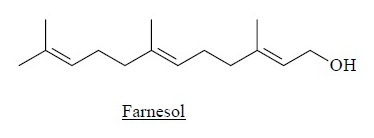
Sobre o composto orgânico farnesol, considere as seguintes afirmativas:
1. A estrutura do farnesol apresenta seis átomos de carbono $sp^2$.
2. O produto de oxidação do farnesol é uma cetona.
3. O farnesol é um álcool insaturado.
4. O composto farnesol apresenta cadeia ramificada.
5. A cadeia hidrocarbônica do farnesol apresenta três ligações duplas na configuração trans.
Assinale a alternativa correta.
Considere as seguintes afirmativas sobre o modelo atômico de Rutherford:
1. O modelo atômico de Rutherford é também conhecido como modelo planetário do átomo.
2. No modelo atômico, considera-se que elétrons de cargas negativas circundam em órbitas ao redor de um núcleo de carga positiva.
3. Segundo Rutherford, a eletrosfera, local onde se encontram os elétrons, possui um diâmetro menor que o núcleo atômico.
4. Na proposição do seu modelo atômico, Rutherford se baseou num experimento em que uma lamínula de ouro foi bombardeada por partículas alfa.
Assinale a alternativa correta.
A mistura de $26,7\ \text{g}$ de $NaCl$ (massa molar $53,4\ g\cdot mol^{-1}$) em água suficiente para que a solução apresente o volume de $500\ mL$ resulta numa concentração de:
A mistura das soluções aquosas de nitrato de prata (massa molar $169,9\ \text{g}\cdot mol^{-1}$) e de cloreto de sódio (massa molar $58,5\ \text{g}\cdot mol^{-1}$) gera uma reação química que produz cloreto de prata (massa molar $143,4\ g.mol^{-1}$) e nitrato de sódio, conforme mostra a seguinte equação química: $$AgNO_{3\ \ \left(aq\right)}+NaC{\ell }_{\ \ \left(aq\right)}\to AgC{\ell }_{\ \ \left(s\right)}+NaNO_{3\ \ \left(aq\right)}$$
Com base nessas informações, considere as seguintes afirmativas:
1. A ocorrência dessa reação química é perceptível devido à formação de um sólido.
2. A massa molar do $NaNO_3$ é $85\ g\cdot mol^{-1}$.
3. Para reagir completamente com $117\ \text{g}$ de $NaC\ell$, serão necessários $339,8\ \text{g}$ de $AgNO_3$.
4. O $NaNO_3$ formado é insolúvel.
5. O $AgC\ell$ é classificado como um sal.
São verdadeiras somente as afirmativas:
Carregando...