UFPR 2015 Química - Questões
Abrir Opções Avançadas
“Gelo de fogo” escondido em permafrost é fonte de energia do futuro? Conhecido como "gelo que arde", o hidrato de metano consiste em cristais de gelo com gás preso em seu interior. Eles são formados a partir de uma combinação de temperaturas baixas e pressão elevada e são encontrados no limite das plataformas continentais, onde o leito marinho entra em súbito declive até chegar ao fundo do oceano. Acredita-se que as reservas dessa substância sejam gigantescas. A estimativa é de que haja mais energia armazenada em hidrato de metano do que na soma de todo petróleo, gás e carvão do mundo. Ao reduzir a pressão ou elevar a temperatura, a substância simplesmente se quebra em água e metano - muito metano. Um metro cúbico do composto libera cerca de 160 metros cúbicos de gás a pressão e temperatura ambiente, o que o torna uma fonte de energia altamente intensiva.
Disponível em: http://www.bbc.co.uk/portuguese/noticias/2014/04/140421_energia_metano_ms.shtml. Acessado em 21/04/2014. Texto adaptado.
Dado: $R=8,2 \times {10}^{-5}\ \text{m}^3\cdot \text{atm}\cdot \text{K}^{-1}\cdot \text{mol}^{-1}$
Para armazenar todo o gás do interior de $1\ \text{m}^3$ de “gelo de fogo” num cilindro de $1\ \text{m}^3$ e a temperatura de $0\ ^\circ\text{C}$, é necessária uma pressão (em $\text{atm}$) de
Águas termais, exploradas em diversos destinos turísticos, brotam naturalmente em fendas rochosas. O aquecimento natural dessas águas, na sua grande maioria, deve-se ao calor liberado em processos radioativos de elementos presentes nos minerais rochosos que são transferidos para a água no fluxo pelas fendas. O gás radônio $(^{222}_{\ }{Rn})$ é o provável responsável pelo aquecimento de diversas águas termais no Brasil. O $\ ^{222}_{\ }{Rn}$ se origina do rádio $(^{226}_{\ }{Ra})$, na série do urânio $(^{238}_{\ }U)$, naturalmente presente em granitos. O tempo de meia vida $\left(t_{1/2}\right)$ do $\ ^{222}_{\ }{Rn}$ é de 3,8 dias, e esse se converte em polônio $(^{218}_{\ }{Po})$, que por sua vez possui um $t_{1/2}$ de 3,1 minutos. Considerando as informações dadas, considere as seguintes afirmativas:
1) A conversão de $\ ^{222}_{\ }{Rn}$ em $\ ^{218}_{\ }{Po}$ é um processo exotérmico.
2) A conversão de $\ ^{226}_{\ }{Ra}$ em $\ ^{222}_{\ }{Rn}$ emite quatro partículas ${\beta }^-$.
3) Na série de decaimento, do $\ ^{238}_{\ }U$ ao $\ ^{218}_{\ }{Po}$, cinco partículas ${\alpha }$ são emitidas.
4) Após 3,8 dias da extração da água termal, a concentração de $\ ^{218}_{\ }{Po}$ atingirá a metade do valor da concentração inicial de $\ ^{222}_{\ }{Rn}$.
Assinale a alternativa correta.
A biodegradação da matéria orgânica produz substâncias húmicas, nas quais os principais componentes são os ácidos húmicos. Estes correspondem a diversas estruturas complexas, que possuem na maioria substituintes fenólicos $(pK_a=8)$ e carboxílicos $(pK_a=4)$. Além de alterar o pH do meio, também são capazes de se ligar a íons metálicos formando coloides. Sobre esse tema, considere as seguintes afirmativas:
1) A presença de substâncias húmicas torna o pH menor que 7.
2) A presença de substâncias húmicas ligadas a íons metálicos é detectada pelo turvamento do meio.
3) O valor medido de pH 6 em uma amostra indica que praticamente todos os substituintes fenólicos estão protonados, enquanto que os substituintes carboxílicos estão desprotonados.
4) O valor medido de pH 4 em uma amostra indica que 50% dos substituintes carboxílicos estão protonados.
Assinale a alternativa correta.
Recentemente, a produção fotocatalítica de hidrogênio vem atraindo atenção devido ao processo que gera um combustível limpo, o qual é utilizado em células a combustível. O processo se baseia na separação da água nos seus componentes, conforme equilíbrio inserido no esquema, utilizando luz solar e um fotocatalisador (p. ex. $NaTaO_3:La$). O processo é extremamente endotérmico, necessitando $1,23\ \text{eV}$ para ocorrer. Num experimento, o processo foi realizado num sistema fechado, como esquematizado abaixo. Considerando essas informações, identifique as afirmativas a seguir como verdadeiras (V) ou falsas (F):
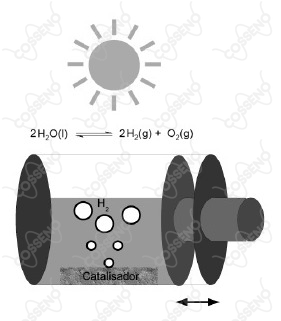
I. ( ) A quantidade de fotocatalisador limita a conversão.
II. ( ) O aumento da temperatura irá favorecer a conversão.
III. ( ) A diminuição do volume do sistema irá favorecer a conversão.
IV. ( ) É condição necessária para a produção de hidrogênio que o fotocatalisador absorva energia solar superior a $1,23\ \text{eV}$.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
O palito de fósforo é um dos artigos mais úteis no nosso cotidiano. Na sua composição, possui fósforo vermelho, enxofre e clorato de potássio. A cabeça de um palito de fósforo pesa aproximadamente $0,05\ \text{g}$. A reação que ocorre na queima da cabeça de fósforo está representada a seguir: $$3P_4+S+10KClO_3+O_2\to 3P_4O_{10}+10KCl+SO_2$$ O cheiro característico de “fósforo queimado” se deve ao dióxido de enxofre formado.
Dados: No palito de fósforo, os componentes estão em quantidades estequiométricas. $M\ (\text{g}\cdot \text{mol}^{-1}):\ Cl=35,5;\ K=39;\ O=16;\ P=31;\ S=32$.
A massa (em $\text{g}$) de dióxido de enxofre produzido ao queimar uma cabeça de fósforo é aproximadamente:
Carregando...