UFPR 2009 Química - Questões
Abrir Opções Avançadas
Segundo o modelo atômico de Niels Bohr, proposto em 1913, é correto afirmar:
Uma solução saturada de $Ag_3PO_4$, a $25 ^\circ\text{C}$, contém 1,2 miligramas desse sal por litro de solução. Assinale a alternativa que apresenta, respectivamente, as concentrações, em $\text{mol}\cdot \text{L}^{-1}$, dos íons $Ag^+$ e $PO^{3-}_4$ e o valor da constante produto de solubilidade $(Kps)$ do $Ag_3PO_4$.
Massas molares: $Ag=107,9\ \text{g}\cdot \text{mol}^{-1};\ P=31,0\ \text{g}\cdot \text{mol}^{-1};\ O=16,0\ \text{g}\cdot \text{mol}^{-1}$.
O gráfico a seguir descreve as variações das concentrações das espécies presentes num sistema reacional, em função do tempo, para a reação hipotética: $$xA+yB\ \ \rightleftarrows\ zC$$
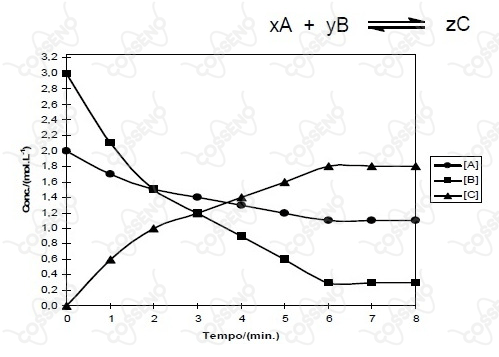
Com base no gráfico, assinale a alternativa que, respectivamente, apresenta os coeficientes $x$, $y$ e $z$ e indica se o valor de $K_c$ é maior ou menor que 1.
$10,00\ \text{mL}$ de uma solução de ${\left(NH_4\right)}_2SO_4$ foram tratados com excesso de $NaOH$. O gás $NH_3$ liberado foi absorvido em $50,00\ \text{mL}$ de uma solução $0,10\ \text{mol}\cdot \text{L}^{-1}$ de $HC\ell$. O $HC\ell$ que sobrou foi neutralizado por $21,50\ \text{mL}$ de uma solução $0,10\ \text{mol}\cdot \text{L}^{-1}$ de $NaOH$. Qual a concentração da solução de ${\left(NH_4\right)}_2SO_4$ em $\text{mol}\cdot \text{L}^{-1}$?
Na produção de alumínio, uma indústria utiliza 15 cubas eletrolíticas em série. Sabendo que a corrente aplicada é $120\ \text{kA}$, qual a massa, em $\text{kg}$, de alumínio produzida por hora?
Dados: Constante de Faraday $\left(F\right)=96.500\ \text{C}\cdot \text{mol}^{-1}$; Massa molar $Al=27,0\ \text{g}\cdot \text{mol}^{-1}$.
Carregando...