UEL 2019 Química - Questões
Abrir Opções Avançadas
O acetato de etila $(CH_3COOCH_2CH_3)$ é um éster simples, usado, no passado, como antiespasmódico e hoje como solvente industrial e removedor de esmalte de unha. A acetona $(CH_3(CO)CH_3)$ também é usada como removedor de esmaltes, mas devido a sua elevada solubilidade em água, quando em contato com a pele, pode desidratá-la.
Sabe-se que estes solventes possuem cheiros parecidos, tornando difícil a identificação pelo olfato.
Considerando um frasco contendo acetato de etila e acetona em quantidades equimolares, assinale a alternativa que apresenta, corretamente, o procedimento para a separação da mistura.
Dados:
Ponto de ebulição do acetato de etila a 1 atm $=77,1 ^{\circ}$C e densidade $= 902$ kg/m$\ ^3$
Ponto de ebulição da acetona a 1 atm $= 56,0 ^{\circ}$C e densidade = 784 kg/m$\ ^3$
Os cosméticos, como batons e rímeis, buscam realçar o encanto da beleza. Porém, o uso desses produtos pode, também, causar desencantamento em função dos constituintes químicos tóxicos que possuem. Em batons, pode haver presença de cádmio, chumbo, arsênio e alumínio. A FDA (Food and Drug Administration) e a ANVISA (Agência Nacional de Vigilância Sanitária) preconizam limites máximos de metais apenas para corantes orgânicos artificiais utilizados como matéria-prima na fabricação de cosméticos.
Considerando que um determinado batom possua concentração de chumbo igual a 1,0 mg $kg^{-1}$ e que a estimativa máxima de utilização deste cosmético ao longo do dia seja de 100 mg, assinale a alternativa que representa, correta e aproximadamente, o número de átomos de chumbo em contato com os lábios ao longo de um dia.
Dados:
Massa molar de chumbo = 207 g $mol^{-1}$
Constante de Avogadro $= 6,0 \times 10^{23}$ $mol^{-1}$
Em 2017, a ANVISA aprovou a administração de um medicamento antirretroviral composto pela combinação das substâncias entricitabina (FTC) e fumarato (molécula contendo ácido carboxílico como função orgânica) de tenofovir desoproxila (TDF) para pessoas com alto risco de infecção pelo vírus HIV. O medicamento apresenta Profilaxia Pré-Exposição (PrEP), ou seja, evita que uma pessoa que não tem HIV adquira a infecção quando se expõe ao vírus.
As estruturas químicas da FTC e do TDF são apresentadas
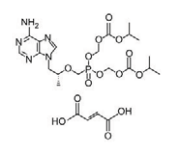
Dados:
Massa molar da FTC = $247,24$ g.mol$\ ^{-1}$
Massa molar do TDF = $635,52$ g.mol$\ ^{-1}$
Sabe-se que a solubilidade em água a $25^{\circ}$C da FTC é $13,4$ mg.L$\ ^{-1}$ e do TDF é $112,0$ mg.mL$\ ^{-1}$ e que a constante de ionização da FTC é de $5,12 \times 10^{-15}$, cujo hidrogênio ácido é aquele pertencente à hidroxila.
Com base nas estruturas químicas e nas informações apresentadas sobre as moléculas, assinale a alternativa correta.
A hipoglicemia é caracterizada por uma concentração de glicose abaixo de $0,70\ \text{g}\cdot\text{L}^{-1}$ no sangue. O quadro de hipoglicemia em situações extremas pode levar a crises convulsivas, perda de consciência e morte do indivíduo, se não for revertido a tempo. Entretanto, na maioria das vezes, o indivíduo, percebendo os sinais de hipoglicemia, consegue reverter este déficit, consumindo de $15$ a $20$ gramas de carboidratos, preferencialmente simples, como a glicose.
A metabolização da glicose, $C_6H_{12}O_6$, durante a respiração, pode ser representada pela equação química de combustão:
$$C_6H_{12}O_{6(s)} + 6O_{2(g)} \to 6CO_{2(g)} + 6H_2O_{(\ell)}$$
No quadro a seguir, são informadas reações químicas e seus respectivos calores de formação a $25 ^\circ$C e $1$ atm:

Sabendo que a massa molar (MM) da glicose é igual a $180,0\ \text{g}\cdot\text{mol}^{-1}$, determine a quantidade aproximada de energia liberada em $\text{g}\cdot\text{mol}^{-1}$ no estado padrão, $\Delta Hr^\circ$, na combustão da glicose, consumida em $350\ \text{mL}$ de refrigerante do tipo Cola, o qual possui, em sua composição, $35\ \text{g}$ de glicose.
Leia o texto a seguir e responda à questão.
Pensem nas crianças
Mudas telepáticas
Pensem nas meninas
Cegas inexatas
Pensem nas mulheres
Rotas alteradas
Pensem nas feridas
Como rosas cálidas
Mas oh não se esqueçam
Da rosa da rosa
Da rosa de Hiroshima
A rosa hereditária
A rosa radioativa
Estúpida e inválida
A rosa com cirrose
A anti-rosa atômica
Sem cor sem perfume
Sem rosa sem nada
A Rosa de Hiroshima. Compositores: Vinícius de Moraes, Gerson Conrad, 1973.
No texto, estão expressos os horrores causados na população de Hiroshima pela explosão da bomba nuclear. Em relação ao princípio físico de seu funcionamento, assinale a alternativa correta.
Carregando...