IME 2016 Química - Questões
Abrir Opções Avançadas
O processo de deposição de filmes finos de óxido de índio-estanho é extremamente importante na fabricação de semicondutores. Os filmes são produzidos por pulverização catódica com radiofrequência assistida por campo magnético constante.
Considere as afirmativas abaixo:
I - O índio é um mau condutor de eletricidade.
II – O raio atômico do índio é maior que o do estanho.
III – A densidade do índio é menor que a do paládio.
IV – O ponto de fusão do índio é maior que o do gálio.
Analisando as afirmativas acima, conclui-se que
Em uma célula a combustível, reações de oxidação e redução originam a uma corrente que pode ser aproveitada, por exemplo, para suprir a potência necessária para alimentar um motor elétrico. Considere um sistema formado por uma célula a combustível que utiliza hidrogênio e oxigênio, acoplada ao motor de um veículo elétrico. Sabendo que o sistema opera sem perdas, que a potência do motor é de $30\ kW$ e que o comportamento do gás ($\ce{H2}$) é ideal, calcule a pressão em um tanque de $100\ L$ de hidrogênio, mantido a $27\ ^\circ C$, de forma que esse veículo percorra um trajeto de $100\ km$ a uma velocidade média de $90\ km/h$.
Identifique a alternativa em que a configuração eletrônica da espécie química representada, em seu estado fundamental, é dada por:
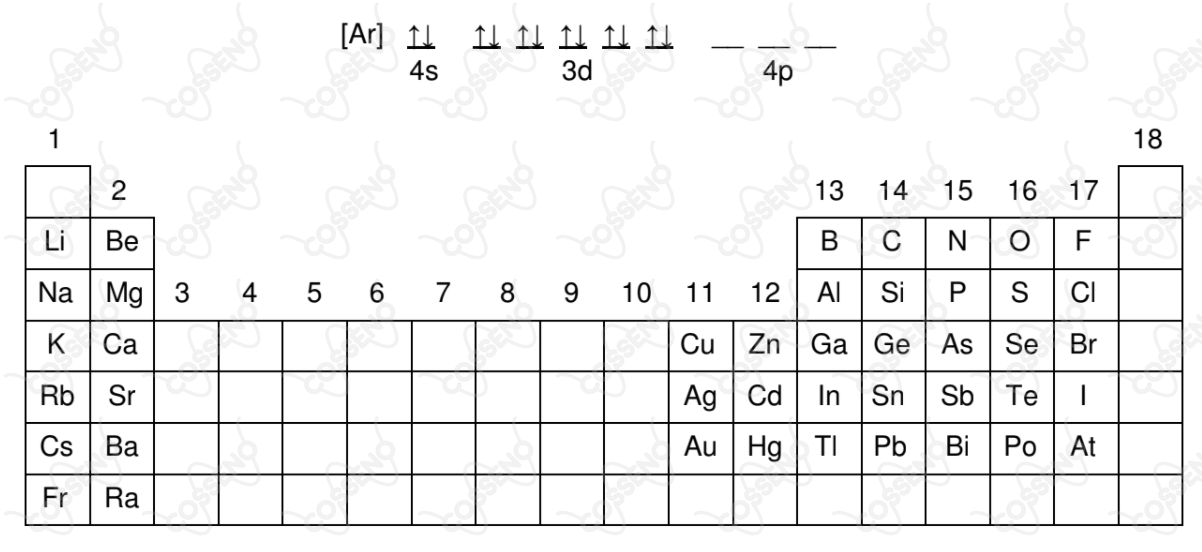
O sulfato cúprico anidro é obtido a partir da reação de uma solução aquosa de ácido sulfúrico $98\ \%$ (em massa), a quente, com cobre. Sabendo que a solução aquosa de ácido sulfúrico tem massa específica $1,84\ g/cm^3$ e que o ácido sulfúrico é o reagente limitante, calcule a massa de sulfato cúprico obtida a partir da reação de $10,87\ ml$ da solução aquosa de ácido sulfúrico.
Assinale a alternativa correta.
Carregando...