ESPCEX 2014 Química - Questões
Abrir Opções Avançadas
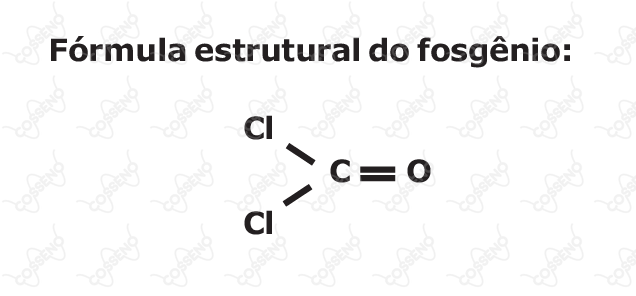
Em um reator foram dispostos $\pu{560 g}$ de monóxido de carbono e $\pu{355 g}$ de cloro. Admitindo-se a reação entre o monóxido de carbono e o cloro com rendimento de $100\%$ da reação e as limitações de reagentes, a massa de fosgênio produzida é de
Considerando os dados termoquímicos empíricos de energia de ligação das espécies, a entalpia da reação de síntese do fosgênio é
Dados:
Energia de Ligação | |
$\ce{C=O}$ | $\pu{745 kJ/mol}$ |
$\ce{C\overleftarrow{=}O}$ | $\pu{1080 kJ/mol}$ |
$\ce{C-Cl}$ | $\pu{328 kJ/mol}$ |
$\ce{Cl-Cl}$ | $\pu{243 kJ/mol}$ |
As substâncias ozônio ($\ce{O3}$); dióxido de carbono ($\ce{CO2}$); dióxido de enxofre ($\ce{SO2}$); água ($\ce{H2O}$) e cianeto de hidrogênio ($\ce{HCN}$) são exemplos que representam moléculas triatômicas. Dentre elas, as que apresentam geometria molecular linear são, apenas,
Um átomo neutro do elemento químico genérico $A$, ao perder $2$ elétrons forma um cátion bivalente, contendo $36$ elétrons. O número atômico deste átomo $A$ é
O cobre é uma substância que possui elevado potencial de redução e no seu estado metálico sofre pouco em termos de oxidação frente a ácidos, não sendo oxidado pela maioria deles. Todavia, ele é oxidado na presença de ácido nítrico, conforme mostra a equação não balanceada de uma das possíveis reações: $$\ce{Cu(s) + HNO3(aq) -> Cu(NO3)2(aq) + NO(g) + H2O(l)}$$ Após o balanceamento da equação com os coeficientes estequiométricos (menores números inteiros) a soma destes coeficientes será igual a
Carregando...